Исследование, проведенное учеными из Массачусетской больницы общего профиля (MGH) и Бригама и женской больницы (BWH), впервые показывает, как мутации, связанные с наиболее распространенной формой наследственной болезни Альцгеймера, вызывают разрушительные эффекты расстройства. Эта статья, появившаяся в выпуске Neuron от 4 марта, переворачивает общепринятые представления о последствиях мутаций, связанных с болезнью Альцгеймера, в генах пресенилина и дает объяснение неэффективности лекарств, предназначенных для блокирования активности пресенилина.
"Наше исследование позволяет по-новому взглянуть на болезнь Альцгеймера, показывая, как мутации человека, вызывающие болезнь, приводят к нейродегенерации и деменции," говорит Раймонд Дж. Келлехер III, доктор медицины, доктор медицинских наук, отделения неврологии и Центра генетических исследований человека в MGH, соавтор статьи о нейронах. "Мы обнаружили, что мутации в гене пресенилина-1 способствуют возникновению характерных признаков заболевания за счет уменьшения, а не увеличения функции белка пресенилина-1 и фермента гамма-секретазы. В дополнение к важным терапевтическим последствиям наших открытий, мы также создали первую модель на животных, в которой мутация, вызывающая болезнь Альцгеймера, вызывает нейродегенерацию в коре головного мозга."
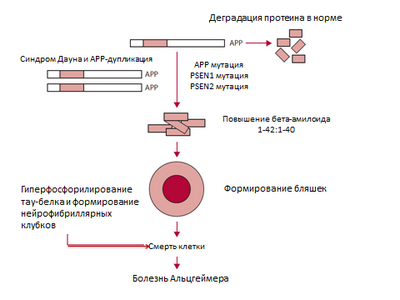
Хотя наследственная или семейная болезнь Альцгеймера (БАД) очень редка и составляет всего около 1% случаев, идентификация более 20 лет назад генов, вызывающих БАД, дала первые ключи к разгадке механизма, лежащего в основе эффектов болезни. Самые редкие мутации, связанные с FAD, обнаруживаются в белке-предшественнике амилоида (APP), который урезается множеством протеаз с образованием бета-амилоидных пептидов, которые накапливаются в амилоидных бляшках, характерных для этого заболевания. Мутации в двух генах пресенилина, которые кодируют важные компоненты гамма-секретазы, одной из протеаз, обрабатывающих APP, составляют около 90 процентов случаев FAD. У людей с пресенилин-ассоциированным FAD симптомы Альцгеймера развиваются даже раньше, чем у людей с мутациями APP.
Хотя механизм, с помощью которого мутации пресенилина вызывают нейродегенерацию, не был известен, общее мнение заключалось в том, что они увеличивают активность пресенилина и гамма-секретазы, что приводит к перепроизводству бета-амилоида и, в частности, бета-амилоида 42, который, как считается, более склонен к осаждение в бляшках. В результате разработка ингибиторов гамма-секретазы стала основным терапевтическим усилием фармацевтических компаний. Но Джи Шен, доктор философии из Центра неврологических заболеваний Энн Ромни при BWH, соавтор статьи о нейронах, поставила под сомнение это широко распространенное мнение и использование ингибиторов гамма-секретазы для лечения болезни Альцгеймера, потому что ее более ранние исследования нормального Функция генов пресенилина показала, что генетическое подавление активности пресенилина и гамма-секретазы у взрослых мышей вызывает нейродегенерацию, подобную болезни Альцгеймера, результаты, которые контрастируют с результатами исследований, в которых перепроизводство бета-амилоида или пресенилинов не приводило к нейродегенерации.
В статье 2007 года, опубликованной в PNAS, Шен и Келлехер, которые лечили пациентов с ФАД с мутациями в гене пресенилина-1 и исследовали механизмы мозга, лежащие в основе когнитивной функции, предложили то, что они назвали гипотезой пресенилина: потеря функции пресенилина может быть первичное событие, вызывающее нейродегенерацию и деменцию при ФАД. В недавних исследованиях Келлехер идентифицировал новую мутацию пресенилина-1, вызывающую FAD, которая инактивировала его функцию в чувствительной системе культивирования клеток. В сотрудничестве с Шеном его группа продолжила показывать, что серия мутаций FAD нарушает функцию пресенилина-1 в культуре клеток.
Эти результаты подняли ключевой вопрос о том, как такие мутации влияют на функцию пресенилина-1 у живых животных, особенно в головном мозге. В то время как в более ранних исследованиях Шен использовались линии мышей, у которых одна или несколько копий генов пресенилина были полностью инактивированы, для этого исследования она и Келлехер создали мышей, у которых были выявлены специфические мутации пресенилина-1, связанные с FAD "постучал в" к гену, заставляя их экспрессироваться так же, как у людей с этой конкретной мутацией. Одна из протестированных ими мутаций относительно распространена среди пациентов с ФАД, а другая – довольно редко; и оба расположены рядом с участком, где белок взаимодействует со своими молекулами-мишенями при включении в гамма-секретазу.
Как и в случае с животными, у которых обе копии пресенилина-1 были удалены в более ранних исследованиях, животные, у которых обе копии были мутированы, не выжили после рождения. Мыши, у которых был мутирован единственный ген пресенилина-1, выжили, но показали недостатки в обучении и памяти по сравнению с контрольными мышами. Производство бета-амилоида в головном мозге этих мышей было фактически снижено, хотя соотношение между формами пептида было изменено, с пропорционально большим образованием бета-амилоида 42, связанного с бляшками. Более тщательное исследование мозга мышей с мутацией FAD показало тот же вид синаптической дисфункции и возрастной нейродегенерации, наблюдаемые в мозге пациентов с болезнью Альцгеймера.
"В этой статье четко показано, что эти мутации FAD вызывают потерю функции пресенилина и активности гамма-секретазы, что приводит к потере нейронов во взрослом мозге," говорит Шен. "Наиболее важным выводом наших результатов является то, что стратегии, которые усиливают, а не ингибируют гамма-секретазу, следует исследовать как потенциальные методы лечения болезни Альцгеймера. Они также могут объяснить, почему крупное клиническое испытание ингибитора гамма-секретазы не помогло пациентам и фактически ухудшило их когнитивные способности." Она добавляет, что их гипотеза пресенилина не исключает роли бета-амилоида в патологии Альцгеймера, она просто помещает активность пресенилина / гамма-секретазы ближе к пути, ведущему к нейродегенерации.
Хотя в этом исследовании изучались только мутации пресенилина-1, отмечает Келлехер, исследователи полагают, что потеря функции является общим свойством мутаций FAD в обоих генах пресенилина. Также необходимо исследование механизмов, лежащих в основе эффектов мутаций АРР, а также изучение того, как дисфункция пресенилина может способствовать распространенной, поздней форме болезни Альцгеймера. "Общие или конвергентные молекулярные пути могут быть ответственны за патогенез как в семейных, так и в спорадических формах, и мы надеемся, что механистические взаимосвязи станут более ясными с идентификацией генетических факторов риска спорадической или поздней болезни Альцгеймера," он говорит. "В настоящее время мы активно реализуем стратегии по разработке возможных методов лечения, восстанавливающих функцию пресенилина-1. Мы также надеемся, что наша модель мыши с нокаутом облегчит разработку и доклинические испытания этих и других агентов, которые могут бороться с нейродегенерацией при болезни Альцгеймера."